9月6日,首个国家亚健康干预技术成果应用中心落户长沙麓谷,国家中医药管理局亚健康干预技术实验室隶属于国家中医药管理局,是国内唯一从事亚健康干预技术研究的专业机构,拥有以国家973项目主持人、教育部新世纪优秀人才为核心的研究团队,专业从事亚健康干预技术的研究。2012年9月,该实验室主任刘东波教授当选为联合国亚太亚健康干预技术联盟主席,以“未病防病、既病防变、愈后防复”为目标,对慢性非传染性疾病提出心理、行为、膳食和营养干预方案,并于2016年成立了国家中医药管理局亚健康干预技术实验室糖尿病干预中心。糖尿病作为实验室创立后的一个重要的慢性病研究对象,历经长期研究,独创了国内第一套糖尿病中医营养干预技术。
刘东波教授文献当中分享了国家中医药管理局亚健康干预技术实验室糖尿病干预中心研究成果。他指出,糖尿病中医营养干预技术就是以三低三高(低血糖负荷、低卡路里、低碳水化合物和高不饱和脂肪酸、高膳食纤维、高药食同源)的饮食模式和间歇性禁食方式治疗糖尿病,以科学的方法为导向,重点教会糖尿病病人正确的健康生活方式,教会他们自我管理血糖的方法,逐步实现恢复胰岛功能,重新夺回控制血糖的主动权,帮助广大糖尿病患者控制病情发展的问题,有利于糖尿病患者科学的自我管理,达到改善健康状况或治疗疾病的目标。
以下是刘东波教授的文献:
H 2 O 2 诱导胰岛 RIN - m5F细胞构建氧化应激模型

摘要:探讨 H 2 O 2 诱导胰岛 β - 细胞氧化应激模型建立。以不同浓度 H 2 O 2 作用于胰岛 RIN - m5F细胞株12 ,18 , 24h探索氧化应激模型;显微镜观察细胞诱导后的形态学变化;采用活性氧( ROS)试剂盒 DCFH - DA 探针检测细胞内活性氧含量; Hochst染色后利用荧光显微镜观察 H2O2诱导后的细胞凋亡情况。结果表明:随着 H 2 O 2 浓度升高,细胞团块减少,崩解增多,细胞数目呈现减少的趋势, ROS含量依次升高,细胞凋亡率增加;随着诱导时间的加长, ROS含量显著增加( P<0.01 )。 250 μ mol / L H 2 O 2 诱导18h是构建氧化应激模型的最佳条件。关键词: H 2 O 2 ;氧化应激;胰岛 β- 细胞
Abstract : To investigate the optimal conditions for oxidative stress
model construction induced by H 2 O 2 in pancreatic β - cell.RIN - m5F
cell was exposed in H 2 O 2 with different concentrations for 12h , 18h ,
24hto construct oxidative stress model.Morphology change was ob -
served by microscope after induction.The content of intracellular re
-
active oxygen species ( ROS ) was detected by DCFH - DA probe in
ROS kit.Cell apoptosis was observed by fluorescence microscope af -
ter Hochst staining.Results : When the concentration of H 2 O 2 rose ,
the cell aggregate abated , disintegration amplified and cell mass pres -
ented a trend of reduction.Meanwhile , the ROS production and ap -
optosis rate increased.Similarly , the ROS production also raised re -
markably as incubation time extended
( P< 0.01 ) .The oxidative
stress model showed perfect state at the H 2 O 2 concentration of
250 μ mol / L after incubation of 18h.
Keywords : H 2 O 2 ; oxidative stress ; pancreatic β - cell
近年来,越来越多的临床和基础研究 [1 , 2 ] 表明,糖尿病及其并发症的发生与氧化应激密切相关。氧化应激是指机体在遭受刺激后,体内活性氧类物质( reactive oxygen species ,ROS )产生过多,如活性氧自由基,超出自身的清除能力,致氧化和抗氧化状态失衡,造成氧化损伤 [3 ] 。与其它组织细胞相比,胰岛 β 细胞由于自身自由基清除酶和 ROS清除蛋白含量较低,在 长 期 高 血 糖 的 诱 导 下 更 易 引 起 氧 化 应 激 反应 [4 ] 。由于糖基化作用、葡萄糖氧化和多元醇等作用导致活
性氧 ROS的产生,胰岛 β 细胞功能损伤甚至细胞凋亡,从而使葡萄糖刺激的胰岛素分泌减少,诱导糖尿病的发生 [5-7 ] 。此外, ROS 还参与一些其它的生物效应,包括细胞的生长、迁移,炎性细胞的表达,基质成分的调控等等,从而导致糖尿病慢性并发症 [8 , 9 ] 。过氧化氢( H 2 O 2 )是一种重要的活性氧物质,它不仅容易发生均裂形成一种活性极强的活性氧自由基———羟自由基( OH ),而且极易透过细胞膜,与细胞内铁离子通过 Fen-ton 反应形成高活性的自由基。同时, H 2 O 2 方便易得、性质稳定,已成为研究细胞氧化损伤的重要工具 [10 , 11 ] 。郑延松等 [12 ] 用低浓度过氧化氢(100 μ mol / L )成功建立了心肌细胞氧化损伤模型, Ankur Maheshwari 等 [13 ] 通过H 2 O 2 体外诱导睾丸精细胞凋亡模型研究其作用途径, F.Warleta 等 [14 ] 研究还发现角鲨烯对 H 2 O 2 诱导的人类乳腺上皮细胞 MCF10ADAN 损伤具有保护作用。但 目 前 为 止,基 于 胰 岛 β 细 胞RIN - m5F 细胞株的氧化应激模型尚未报道。胰岛素瘤是起源于胰岛 β 细胞最常见的一种胰腺内分泌肿瘤,其不依赖血糖变化而分泌和释放过量的胰岛素,因此近年来常用作胰岛β 细胞的体外模型进行糖尿病的机理研究。本研究拟通过不0 4同 H2 O 2 浓度诱导胰岛 β 细胞 RIN - m5F细胞株不同的时间,观察其细胞形态,检测其活性氧水平,细胞凋亡数目,建立体外氧化应激模型,为续抗糖尿病的药物筛选及药理评估提供依据。
1 材料与方法
1.1 试验材料
1.1.1 细胞株
大鼠胰岛素瘤细胞株 RIN - m5F :派通(上海)生物科技有
限公司。
1.1.2 主要试剂耗材与仪器胰蛋白酶( Trypsin ):≥3 000U /mg,德国Sigma公司;活性氧( ROS )测试盒:南京建成生物工程研究所;胎牛血清、 RPMI- 1640培养基:美国 Hyclone公司;6孔细胞板、 96孔细胞板、培养瓶:美国康宁公司;精密电子天平: PL403型,瑞士 Mettler Toledo公司;移液枪:lh - 212型,德国 Eppendorf公司;CO 2 恒温细胞培养箱: 2424 - 2 型,美国 Shellab 公司;细胞计数仪: Countess 型,美国 Invitrogen 公司;全波长多功能酶标仪: THERMO Multiskan Flash 型,芬兰 Labsystems 公司;荧光倒置显微镜:IX71 型,日本 Olympus 公司。1.2 试验方法
1.2.1 细胞培养 RIN - m5F 细胞株复苏后用含 15% 胎牛血清的 RPMI1640 培养基转入培养瓶中,于 37℃ 、 5% CO 2 、具有饱和湿度的 CO 2 培养箱中培养。次日经 5% 胰酶消化后,更换含 13% 胎牛血清的 RPMI1640 培养基以 1∶3 的比例进行传代培养, 4 代后的对数期细胞用于以下试验。
1.2.2 细胞分组 取第 4 代后对数期生长细胞,消化后按1×106 个细胞/孔接种于 6 孔板或 1×10 4 个细胞/孔接种于96 孔板(细胞密度由细胞悬液加入胎盼蓝于细胞计数仪直接读取),贴壁培养。细胞分组:
( 1 )空白对照组:13% 胎牛血清的 RPMI1640 培养基;
( 2 )对照组( A ): 13% 胎牛血清的 RPI1640 培养基 +定量等体积 DMSO ;
( 3 )模型对照组( B ): 13% 胎牛血清的 RPMI1640 培养基 +100 μ mol / L 活性氧供氢体(试剂盒提供) + 定量等体积DMSO ,作为构建模型的阳性对照;
( 4 )模型组1 ( C1 ): 13%胎牛血清的 RPMI1640培养基+100 μ mol / L H 2 O 2 +定量等体积 DMSO ;
( 5 )模型组 2 ( C2 ): 13% 胎牛血清的 RPMI1640 培养基+175 μ mol / L H 2 O 2 + 定量等体积 DMSO ;
( 6 )模型组 3 ( C3 ): 13% 胎牛血清的 RPMI1640 培养基+250 μ mol / L H 2 O2 +定量等体积 DMSO ;
( 7 )模型组 4 ( C4 ): 13% 胎牛血清的 RPMI1640 培养基+325 μ mol / L H 2 O 2 + 定量等体积 DMSO ;
每组在分别培养 12 , 18 , 24h 后进行后续试验(分别标记为-1, -2 , -3 ),每一时间点3个重复。 DMSO的加入,用来消除后续研究药物溶解带来的系统误差。
1.2.3 细胞形态学观察 置显微镜10×目镜,10×物镜下观察结果及拍照。
1.2.4 活性氧检测 参照试剂盒说明书,取各处理组细胞,吸弃培养基, PBS冲洗2次后,加入10 μ mol / L的DCFH - DA探针工作液。黑暗中37℃孵育1h ,使用全波长多功能酶标仪上机检测,其中激发波长488nm ,发射波长525nm 。
1.2.5 荧 光 显 微 镜 观 察 细 胞 凋 亡 将 Hochst 33342( 1mg / mL ,pH 7.0)加入培养的 RIN - m5F细胞中至终浓度10 μ g / mL ,避光37 ℃孵育30min ; 100 μ g / mL 多聚赖氨酸和PBS以1∶9的比例混合,包被细胞5min 。在荧光显微镜10×目镜, 10×物镜下观察,荧光显微镜激发滤片选用紫外光( UV)激发滤片,阻断滤片为460nm 。1.2.6 数据统计试验结果使用 Excel 2003和SPSS 19.0软件进行统计学方差分析,所得数据以平均数±标准差表示。各组均数均采用 LSD ( Least - significant difference test ),其中 P<0.05 为显著差异有统计学意义, P<0.01 为极显著差异。
2 结果与分析
2.1 细胞形态与细胞数目观察
显微镜观察细胞形态结果显示:正常胰岛 β 细胞呈单层贴壁生长,细胞间有连接并部分融合成岛状,细胞边缘清晰,呈多边不规则形,分布均匀,生长良好。模型对照组,加入活性氧供氢体后,细胞贴壁性能变差,重叠处减少,散状分布增多。而经 H 2 O 2 诱导后的胰岛 β 细胞,细胞间连接明显减少,细胞呈钝圆,少触角;但模型组各梯度、各时间段的形态,由肉眼观察无法鉴定是否具显著性差异。同时,据图 1 观察可知,模型组与模型对照组的细胞密度均小于对照组。
2.2 H 2 O 2 诱导的 RIN - m5F 细胞 ROS 检测DCFH - DA ( 2 ’, 7 ’ - dichlorofluorescein diaceate )是迄今最常用、最灵敏的细胞内活性氧检测探针, DCFH - DA 本身没有荧光,进入细胞后被酯酶水解为 DCFH ( dichlorofluo -rescein ),当活性氧存在时 DCFH 被氧化为不能透过细胞膜
的强绿色荧光物质 DCF ( dichlorofluorescein )被荧光酶标仪检测。由表 1 可知,对照组与空白对照组相比,无论时间长短, ROS含量均有所上升,但不具有统计学差异;而与对照组相比,模型对照组 ROS含量极显著上升( P<0.01 ),模型组3、4 ( 250 , 325 μ mol / L H 2 O 2 )不同的处理时间组其ROS含量均极显著上升( P<0.01 )。当 H 2 O2 处理时间为 12h ,模型组 3 、 4 ( 250 , 325 μ mol / L H 2 O 2 )其 ROS 含量极 显 著 上 升( P<0.01 );而各浓度处理 24h 后,虽均具有极显著差异,ROS含量上升( P<0.01 ),但是随着处理浓度逐渐增加至325 μ mol / L 时,其 ROS 含量却有下降的趋势。当 H 2 O 2 诱导时间为 18h ,各模型组间表现出差异性,除模型组 1 外,其余组 ROS 含量均显著上升,诱导浓度 175 μ mol / L 具有显著性。

图 1 不同处理组胰岛 RIN - m5F 细胞株形态学的观察
Figure 1 Morphology of pancreatic RIN - m5Fcelllines in different treatment表 1 H 2 O 2 对 RIN - m5F 细胞 ROS 含量的影响 Table 1 Effect of H 2 O 2 on ROS contentin RIN - m5Fcell ( n =3 )
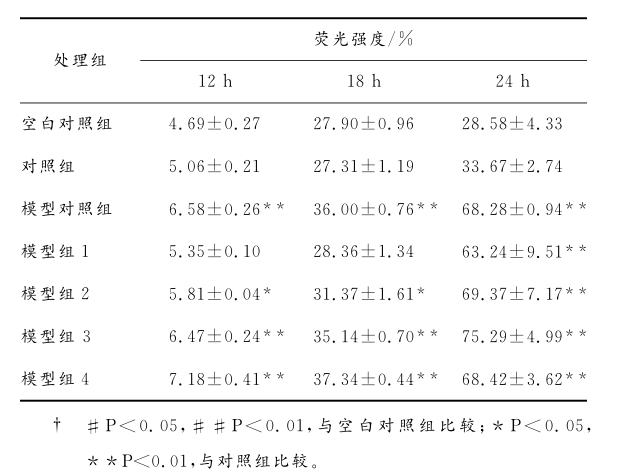
差异( P<0.05 ),浓度为 250 ,325 μ mol / L 时具极显著差异性( P<0.01 )。
2.3 荧光显微镜观察细胞凋亡
Hochst 33342 可被细胞摄取,与 DNA 结合在紫外光下
呈蓝色荧光。在荧光显微镜下,活细胞核呈弥散、微弱、均匀荧光,坏死细胞不被 Hochst染色,凋亡细胞由于对 Hochst摄取增强,其细胞核或细胞质内可见浓染致密的颗粒状荧光(蓝色)及明显核形态变化 [15 ] 。本试验中,对照组呈现弥散、微弱的蓝斑; H 2 O 2 诱导RIN - m5F细胞株,随着 H2 O 2 浓度的增加其细胞可见浓染致密的蓝色斑点数目增加,即细胞凋亡的数量大幅增加,且趋势呈剂量依赖性(图 2 )。

图 2 H 2 O 2 诱导胰岛 RIN - m5F 细胞株 Hochst 染
色后荧光显微镜的观察(诱导 18h )
Figure 2 H 2 O 2- induced pancreatic RIN - m5Fcell
apoptosis observed by fluorescence
microscope after Hochst staining
3 讨论
氧化应激诱导产生的过量 ROS 不仅可以直接损伤胰岛β 细胞,还可以通过影响胰岛素合成和分泌的信号转导通路间接损伤胰岛 β 细胞 [16 ] 。因此探讨胰岛 β 细胞氧化应激模型对糖尿病的研究具有重要意义。
本试验采用 H 2 O 2 诱导胰岛 β 细胞建立氧化应激模型。由显微镜观察结果可知, H 2 O 2 诱导后胰岛 β 细胞形态呈现凋亡状态,且与正常对照组细胞相比,细胞数目明显减少,说明 H 2 O 2 可较好地诱导构建氧化应激模型;但各 H 2 O 2 诱导浓度与诱导时间点其细胞形态与细胞数目,由肉眼观察无法鉴定是否具显著性差异,因此本研究进行了 H 2 O 2 诱导后的活性氧检测。
在所有时 间 处 理 组 中,模 型 组 3 、 4 ( 250 , 325 μ mol / LH 2 O 2 )的 ROS含量均极显著上升( P<0.01 ),但仔细观察发现, 325 μ mol / L H2 O 2 诱导 24h 后活性氧含量减少,呈下降趋势。这可能是由于过量的 H 2 O 2 导致了细胞的大量凋亡,从而使 ROS含量的测量值降低。本模型的构建是为了方便后期抗糖尿病药物的抗氧化性研究,因此,本研究构建的氧化应激模型的理想状态是,细胞 DNA 被外泄、损伤,细胞内的脂质、蛋白质也被破坏,这种损伤可能会导致细胞凋亡,但在适宜的抗氧化剂的作 用 下,却又 有 可 能 被 修 复。因 此,250 μ mol / L H 2 O 2 可作为氧化应激的最佳浓度,此浓度可较好地诱导胰岛 RIN - m5F细胞损伤( P<0.01 ),却又避免了浓度过高导致的细胞不可逆损伤。由于250 μ mol / L H 2 O 2 各诱导时间处理组( 12 ,18 , 24h )其 ROS含量均大幅上升( P<0.01 ),考虑到12h的 ROS测量数值较小且试验时间不易安排, 24h诱导时间过长,也有可能会导致过度损伤,因此本试验选定18h作为最佳诱导时间。在获得了构建氧化应激模型的最佳诱导浓度250 μ mol / LH 2 O 2 和诱导时间18h后,本试验还采取 Hochst 33342荧光染色观察细胞凋亡状来验证本氧化应激模型。由图2可知,随着 H 2 O 2 浓 度 增 加,细 胞 凋 亡 数 量 呈 上 升 趋 势,浓 度 达325 μ mol / L时,细胞大量凋亡。从而可知, 250 μ mol / L H 2 O 2诱导胰岛 RIN - m5F细胞18h可较好的构建氧化应激模型。目前,已有文献报道 H 2 O 2 诱导构建的多种细胞氧化应激 [17 ] ,其选择 H2 O 2 诱导浓度各异, 1 μ mol/ L 至4mmol / L不等 [18 ] ,而 诱 导 时 间 也 各 不 相 同,自 10 min 至 24h 不等 [19-21 ] 。叶春 玲 等 [ 22 ] 以500 μ mol / L H 2 O 2 作 用 于 胰 岛RIN - m β 细胞 6h 建立凋亡模型,与本试验所得结果相近。而张健等 [21 ] 构建血管内皮细胞的氧化应激损伤模型只采用了 1 μ mol / L H 2 O 2 培养 4h ,庹勤慧等 [23 ] 却利用高浓度 H2 O 2( 1mmol / L )诱导 24h 构建血管内皮细胞凋亡模型。这可能是由于所诱导的细胞/细胞株系、细胞的培养条件、试验的环境以及试验目的各不相同。氧化应激与糖尿病的发生密切相关,合适的细胞模型对体外评价对其发病机制及抗糖尿病的药物作用机理研究有着重要的指导意义。该模型的建立为揭示糖尿病氧化应激机制以及研究和筛选抗氧化药物和功能食品奠定了基础。
参考文献
1 Amira A M Adly.Oxidative stress and disease : an updated re -view [ J ] .Research Journal of Immunology , 2010 , 3 ( 2 ): 129~145.
2 Eardoun R Z.The use of vitamin E in type 2diabetes mellitus
[ J ] .Clin Exp Hypertens , 2007 , 29 ( 3 ): 135~148.
3 Turko I V , Mareondes S , Murad F.Diabetes - associated nitra -tion of tyrosine and inactivation of succinyl - CoA : 3 - oxoacid CoA -
transfersse [ J ] .Am.J.Physiol Heart Circ Physiol , 2001 , 281
( 6 ): H2 289~2 294.
4 Dave G S , Kalia K.Hyperglycemia induced oxidative stress in
type - 1and type - 2diabetic patients with and without nephropathy
[ J ] .Cell Mol Biol. , 2007 , 53 ( 5 ): 68~78.
5 A C Maritim , R A Sanders , J B Watkins III.Diabetes , oxidative
stress , and antioxidants : a review [ J ] .J.Biochem.Molecular
Toxicology , 2003 , 1 ( 17 ): 24~38.
6 Evans J L , Goldfine I D , Maddux B A , et a1.Oxidative stress
and stress - activated signaling pathways : a unifying hypothesis of
type2diabetes [ J ] .Endocr Rev , 2002 , 23 ( 5 ): 599~622.
7 Piro S , Anello M , Di Pietro C , et al.Chronic exposure to free
fatty
acids or high glucose induces apoptosis in rat pancreatic is -
lets : Possible role of oxidative stress [ J ] .Metabolism , 2002 , 51
( 10 ): 1 340~1 347.
8 Brownlee M.The pathobiology of diabetic complications : a unif -
ying mechanism [
J ] .Diabetes 2005 ( 54 ): 1 615~1 625.
9 Giuseppe Castello , Susan Costantini , Stefania Scala.Targeting
the inflammation in HCV - associated hepatocellular carcinoma : a
role in the prevention and treatment [ J ] .Journal of Translational
Medicine , 2010 ( 8 ): 109~120.
10 Hampton M B , Orrenius S.Dual regulation of caspase activity
by
hydrogen peroxide : implication for apoptosis [ J ] .Febs Lett ,
1997 , 414 ( 3 ): 552~556.
11 源瀚祺,黄庆华,李娆玲 .通过细胞模型体外评价抗氧化活性实验方法研究综述[ J ] . 广东药学院学报,2012 , 28 ( 2 ): 208~211.
12 郑延松,李源,张珊红 .用低浓度过氧化氧建立心肌细胞氧化损伤模型[ J ] . 第四军医大学学报,2001 , 22 ( 20 ): 1 849~1 851.
13 Maheshwari A , Misro M M , Aggarwal A , et al.Pathways in -volved in testicular germ cell apoptosis induced by H 2 O 2 in vitro[ J ] .FEBS , 2009 ( 276 ): 870~881.
14 Fernando Warleta , María Campos , Yosra Allouche , et al.Squa -
lene protects against oxidative DNA damage in MCF10Ahumanmammary epithelial cells but not in MCF7and MDA - MB- 231human breast cancer cells [ J ] .Food and Chemical Toxicology ,2010 ( 48 ): 1 092~1 100.
15 胡野,凌志强,单小云 .细胞凋亡的分子医学[ M ] . 北京:军事医
学科学出版社, 2002 : 471~475.16 Robertson R P , Harmon J , Tran P O , et al.Glucose toxicity inbeta - cells : type 2diabetes , good radicals gone bad , and the glu -tathione connection [ J ] .Diabetes , 2003 ( 52 ): 581~587.
17 杨丽娟,游育红 .
细胞受到氧化应激后损伤的检测方法[ J ] . 医学综述, 2010 , 6 (16 ): 924~927.
18 齐晓龙,赵芹,张亚男,等 .过氧化氢诱导产蛋鸡原代肝细胞氧化应激模型的建立[ J ] . 营养饲料,2013 , 49 ( 11 ): 49~52.
19 李军华,何小飞,徐细明,等 .雷公藤多苷对溃疡性结肠炎大鼠一氧化氮和一氧化氮合酶的影响 [ J ] . 医 药导 报, 2004 , 23 ( 5 ):300~302.
20 赵翠翠,张锦,刘凤芝,等.山奈酚、芹菜素对 H2 O 2 诱导的心肌细胞凋亡过程中线粒体损伤的影响[ J ] . 中国病理生理杂志,2008 ,24 ( 7 ): 1 431~1 433.
21 张健,魏欣冰,丁华,等.卡维地洛对过氧化氢致血管内皮细胞氧
化应激损伤的保护作用[ J ] . 中 国 药 理 学通 报, 2006 , 22 (
5 ):620~624.
22 叶春玲,金永亮,叶开和,等 .银杏提取物对 H 2 O 2 诱导的胰岛
Rinm β 细胞凋亡的影响[ J ] .中药材, 2007 , 30 ( 4 ): 424~428.23 庹勤慧,朱炳阳,廖端芳,等 .金粉蕨素抑制氧化应激诱导的血管内皮细胞凋亡[ J ] .中国动脉硬化杂志,2004 , 12 ( 3 ): 283~28







